

TOPICS
CHNフォーラム
第十一部 CHN計算法の進歩
- 1-1.はじめに
- 2-1.元素含有率の計算 計算の精度
- 2-2.元素含有率の計算 計算の用具
- 2-3.元素含有率の計算 論理回路
- 3-1.定量分析の計算 計算目的の多様化
- 3-2.定量分析の計算 自己積分法のモル分率補正
- 3-3.定量分析の計算 モル分率補正法の改革
- 3-4.定量分析の計算 モル分率補正式の直接解法
- 4-1.おわりに
- 5-1.参考文献
- 関連装置
1-1.はじめに
定量分析は数値を出すことが主目的ですが,数値には精度,真度,不確かさなどいろいろな質的評価がされます.標準試料のようにあらかじめ成分の含有率が分かっているときは,それを基準に分析結果の良い悪いを評価することが出来ますが,未知試料では分析値を出しても推定化学構造が間違っていたり,不純物が含まれていたりすることもあり,結果がこれで正しいのか判定が難しくなります.最近は核磁気共鳴や質量分析装置などスペクトル解析が普及して,試料の化学構造が簡単に分かるようになっていますが,不純物があってもそのスペクトル強度が小さいので普通見落とされてしまい,構造の解析には支障がありません.ところが有機元素分析では試料中の成分全体の含有率を測定するので,不純物があれば予想含有率と少し異なる分析値を与えます.スペクトルに頼る有機化学者には元素分析値だけがおかしいとクレームをつけられることもありますが,不純な試料をそのまま通さないための関所として大事な役目を有機元素分析は果たさなければなりません。
リービッヒによるCH分析法の開拓以来,ジュマのN分析,カリウスのハロゲン硫黄分析と広がって来ましたが,プレーグルの微量化で一連の分析技術が整備され,これによって生化学,天然物化学が大きな発展を遂げました1)。しかし最も初期から試料中の元素成分の含有率を求める計算は現在も延々と続けられています。計算が加減算より乗除算を多く使うことから,筆算で結果を求めるのは分析者にとって大きな負担でした.3~4桁の乗除ですから途中の誤算,転記ミスも多く,そのうち対数表を利用して乗除算を加減算に変換し,あとで真数を求めるようになりました。
aF/b=c → loga + log F - logb= log c
第二次大戦のあと暫くまではどの分析化学の教科書にも巻末に対数表が掲載されていて,定量分析の結果は対数計算で行うというのが常識でした。(図1)それでも対数表の数値を探して書き取り,互いに足したり引いたりを筆算で行うのですから,その煩わしさはかなりのものです。分析装置も現在のように自動ではありませんから,試料の燃焼や装置の操作につききりとなり,ゆっくり計算している暇がありません。分析結果に疑問がでたら,計算ノートをもう一度見直して検算する必要があり,一日の仕事がなかなか終わらないこともよくありました。
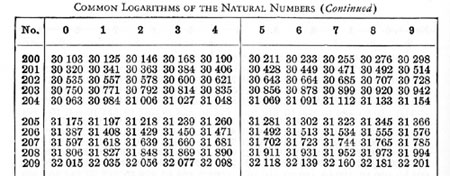
図1 5桁対数表
加減算に機械式の計算機を最初に考案したのは, 有名なフランスの哲学者パスカル(B. Pascal, 1623―1662)で,税官吏の父の業務計算を助けるためであったと言います。その後ドイツのライプニッツ(G. W. Leibniz, 1646―1716)が乗除算に使える機械を作ったものの,歯車がうまく作動せず,全く普及しなかったようです。
1891年スエーデンのオドナー(W. T. Odhner)が実用品の製作に成功し,はじめて世界中で使われるようになりました。わが国では大阪で機械工場を経営していた大本寅治郎(1887―1961)が1924年オドナー型のものを作り,「寅」の字を入れてタイガー計算機の名で売り出しました。(図2)しかし当時としてはかなり高級な器械で,誰でも持てるものでなく,一般分析室では対数表が引き続き使われていました.戦後の復興が始まって1950年ごろからようやくタイガー計算機や後発の日本計算機が普及し始めましたが,初めて使ったときはすばらしい新兵器を手に入れたように思いました。ハンドルを回すときに歯車の音がガラガラと喧しい器械でしたが,対数表を使う煩わしさがなくなり,分析計算は随分楽になりました。この頃分析装置も試料自動燃焼の時代になり,装置につききりという拘束からも外れ,分析室はかなり快適な仕事場になったように思います。

図2 タイガー計算機
それから半世紀,熱伝導度法によるCHN分析装置が開発され,分析が高速化されると共に,タイミングよく電子部品や集積回路の進歩で演算機能を持った小型の電子計算機が次々と導入され,ボタン操作で計算結果を表示してくれるようになりました。装置の検出器から出されるシグナルは,単なる電気信号ですから,これを試料中の元素含有量に正確に対応させ,分析データとするため補正など少々面倒な演算をしなければなりません。予め仕組まれた演算プログラムが開発され,付属装置のコンピュータによって分析結果がプリンタに打ち出されます。最近は分析装置の運転までコンピュータ指令に基づいて出来るようになって,電子装置への依存度が高まっています。計算法の細かい点についてはまだ問題点も残されていますが,常用分析には十分受け入れられるものになっていると思われます。初期から現在までどのように計算法が進歩したかを辿ります。
2-1.元素含有率の計算 計算の精度
有機物の化学構造は1分子の原子構成を表したものですが,純粋な物質であれば全部の分子が同じ化学構造のはずで,適当な量の試料をとってその中の元素組成を測定すれば,1分子の化学組成と同じになります。元素組成を測定すると言っても元素を直接取り出すことは出来ませんから,燃焼や熱分解で決まった化学形に変え,その量から元素の質量を計算し試料中の元素組成%を求めることになります。この元素組成を予想化学構造から計算される理論値と比べて,予想が正しかったかどうかを判定しますが,元素の含有率を知るためには基本的にこの計算が必要で,計算法がどのように進歩してもこの原則は変わりません。
標準試料のように純粋なものは理論値が分かっていますが2),それでも実際に分析してみると一回の分析値は理論値に正確には一致せず,繰り返し分析によってばらつきを持ったデータが得られます.個々の分析値では判断できない試料の純度が,統計手法でより正しく判定されますが,これにも繰り返し分析の精度や不確かさなど結構面倒な計算が必要となって来ます3)。不純物を含む試料では予想含有率を少し外れた分析値が得られやすいのですが,原因について試料の不純によるのか,分析の不手際によるのか水掛論になることがよくあります。そう言うとき分析担当者の自衛手段として構造の近い標準試料を繰り返し分析して,データ群の標準偏差から現状の分析値のばらつきを知っておき,未知試料の分析値と予想含有率の差つまり誤差を不確かさの確率をつけて報告することが出来ます。ばらつきの大きい分析装置では誤差があっても不確かさの範囲(95%の確率で含まれるばらつきの限界)に入ってしまって,未知試料が予想の構造と違っているとは言えないことになります.逆にばらつきの小さい装置では不確かさの範囲より誤差のほうが大きいので,明らかに予想の構造と違うか,または不純物が含まれていると言う事ができます。
定量分析ですから扱う数値の桁数は大きいほどよいのですが,測定器の能力で限界があります。試料の計量ははかりによって行われますが,マクロ分析では200~500 mgを化学はかりで量るので,読み取り精度は0.1 mgとなり,4桁の数値になります。試料が2~5 mgの微量分析では微量化学はかりを用い,読み取り精度は1μgですからやはり4桁の数値を扱うことになります。最近は電子はかりが一般的になってきて,長い歴史を持つ機械式はかりはほとんど姿を消してしまい,一方電子はかりは電気的拡大が容易なことから,微量はかりをさらに改良した超微量はかりと称する読み取り精度0.1μgのものもよく使われるようになり,最終桁の繰り返し精度に問題はありますが,一応5桁の計量値が得られます。
読み取り精度には当然ばらつきがあり,しかも実際の分析では空の試料ボートを量ったあと,試料を入れてもう一度計量し,その差を試料量とするのですから,ばらつきが2回重なります。はかりのばらつきが標準偏差でσとすると分散はσ2ですから,試料量のばらつきσ0は次のようになります4)。(5:分析値の信頼性; 3.1 サンプリング誤差を参照)
σ02 = 2σ2 ∴σ0 = 1.41σ
4桁の数値は1/1000より高い判定能力があり,微量分析で3 mgの試料を採取すれば数値上1/3000まで精密測定ができることになります。しかしはかりのばらつきがありますから,もしその値がσ=1.5μgであればサンプリング誤差は
σ0=1.41σ=2.13μg
となり,目算どおりの精度で測定は出来ませんが,それでも1/1000に割合近い精度で試料の計量ができると思われます。
2-2.元素含有率の計算 計算の用具
CH分析やN分析を手作業で実施していた頃は,燃焼成分を吸収管やガスビュレットに採取して質量や体積を求めていました。例えばショ糖 (C12H22O11) 3.025 mgを燃焼して吸収管の増量がH2O=1.752 mg,CO2=4.671 mgであったとすると,これから元素の質量を知るには,H2/H2O=0.1119とC/CO2=0.2729の係数が必要です。対数表を使って計算を進めるときは,
H%=1.752×0.1119×100/3.025
C%=4.671×0.2729×100/3.025
ですから,
logH%=log1.752 + log11.19-log3.025=0.2435 + 1.0488-0.4807 = 0.8116
logC%=log4.671 + log27.29-log3.025=0.6694 + 1.4360-0.4807 = 1.6247
対数表ではまず真数の小数点を無視した値から求めた対数値(仮数)が記載されていて(図1),あとで小数点の位置を決めます。例えばlogH%の計算式では1752の対数が2435(仮数)ですが,真数1.752が1より大きく10より小さい値,つまり100~101の値ですからlog1.752=0.2435となります。同様に11.19は10より大きく100より小さい値,つまり101~102の値ですから log11.19=1.0488となります。
得られたlogH%=0.8116とlogC%=1.6247は小数点以上がそれぞれ0と1ですから真数の小数点以上はそれぞれ1桁と2桁です。そこで今度は対数の仮数の値を見て,対数表からそれぞれの真数を探すと6481と4214が得られますが,小数点以上が1桁と2桁ですから
H%=6.48 C%=42.14
となります。一分析毎にこのような面倒な計算を進めるのは大変ですが,それでも紙の上で4桁の乗除算をするより大分楽で,定量分析には長い間この対数計算が利用されました。ただし毎日このような決まった計算をしていると,小数点位置などあまり気にしなくても出来るようになります。
江戸期から「読み書きそろばん」と言われましたが,計算手段としてのそろばんは日常生活に大切なものでした。そろばんの語源は中国語の「算盤(スアンパン)」から来たものと言われますが,本来は加減算に向いたもので特に商人には帳簿の記入に重宝しました。和算家によって乗除算にも応用できるようになりましたが,「二一天作の五」など符丁を使って入力して行くので,誰でも操作できるものではありません。(図3)

図3 和算書
しかし中には乗除算が得意な方もあって,分析室で場違いなそろばんの音を響かせることもありました.この外にも手軽な道具として計算尺slide ruleというものが1850年ごろフランスで実用化されましたが,これは真数を対数の間隔に目盛りとして刻んだもので,2本の物差しを滑らせて対数の和または差を求めます。(図4)

図4 計算尺
しかし目盛りには真数の値が刻んであるので,読み取り値は真数の乗除になります。
この計算尺は明治の末期に逸見治郎(へんみじろう)によって国産化され,日本の竹の真っ直ぐな性質を利用して国際的にも優秀な製品に仕上げられました。計算尺は長いほど精密な数値が得られますが,普通使われている25cm程度のものではせいぜい3桁の計算しか出来ませんので,定量分析には概算用に使われただけでした。
機械式の計算機の発明は本稿の冒頭にも触れましたが,オドナー計算機が世界的に普及し,そのレプリカとも言える国産品のタイガー計算機が生産され,乗除算が一挙に簡単迅速になりました。最初に被乗数を置数しておいてレバーを時計回りに回転すると回転数が乗数になり左ダイヤルに表示されます。下の桁から上へ順にずらしながら掛けて行くと積が右ダイヤルに示されます.除算は反対にレバーを反時計回りに回転して実行できます。この手回し計算機はその後電動式のモンロー計算機などが現れ,価格はかなり高いものでしたが,予算のある事業所ではある程度使われるようになりました.銀行など預金や投資の利回り計算には随分役に立ったと思われます。
機械式計算機はそれなりの発展を遂げていたのですが,電子計算機の出現で突然と言えるほど急速に消滅しました。もともと電子計算機の開発のきっかけは第二次大戦中,海軍の大砲の射撃角度を瞬時に計算したいとの要望からですが,真空管を用いて複雑な計算プログラムを実行させようとしました。結局終戦までには間に合いませんでしたが,1946年ペンシルバニア大学で1万8000本の真空管を使って最初の電子計算機 ”ENIAC” が作られ,(図5)以来これを改良発展させた機械がコンピュータと名づけられて続々市場に現れました。

図5 真空管式電子計算機 ENIAC
しかしこのコンピュータの出現とその後の小型化には大きな二つの要素が支えになっています。まずコンピュータが作動するには論理回路というネットワークが必要ですが,これの基礎理論を作ったのは英国のブール(George Boole, 1815~1864)です。ブールは200年も前にすでに二進法を用いていろいろな計算を論理式で表現できるようにしました。もう一つの要素はトランジスタを含む半導体集積回路の製造技術です。
2-3.元素含有率の計算 論理回路
二進数は0と1で成り立っていますから,0×0=0,0×1=0,1×1=1の論理積があります。また0+0=0, 0+1=1,1+1=(2) ですが (2) が無いので桁上がりをして1+1=10という論理和になります。十進数の0~10を二進数で並べると,
0 1 10 11 100 101 110 111 1000 1001 1010
となり,十進数より桁数が多くなりますが,各桁の積や和は計算というより簡単な約束だけで答えが出てきます。もう少し機能を拡大すると否定(1を入力すると答えは反対の0,0を入力すると答えは1)やこれを使った排他的論理和(1と0を入力したときのみ答えは1,また0と0や1と1を入力すると答えは0)などが構成できます。一桁の加算を行う電気回路を半加算器といいますが,論理回路のブロックで表すと図6のようになり,ここでA, Bに0 か1を入力すると三角で示した否定回路で反転され,論理積の回路に入ります.その結果を論理和の回路に入れると排他的論理和の答えSになります。AもBも1のときはその桁は0ですが,横に論理積の回路を設けておくと桁上がりCが判定され,上の桁に1が加わります。
基本論理を紙の上で方程式のように並べて書いて,それぞれの論理を実行する電気回路をあてはめて設計図に描けば,どんなに複雑な命令でも目的どおり働きます。発案者の名前を取ってブール代数(Boolean algebra)という数学理論に纏め上げられていますが,昔のことですから当時は実用にもならず,すばらしい発明をしたのに成果が認められず気の毒なことでした。今日のコンピュータ技術を底辺から支えている画期的な理論ですから,ノーベル賞なら二つ三つに値する貢献です。余談ですが,ブールはイギリス中部の田舎町リンカーンで貧しい商家に育ち,小学校を出ただけですが,16才から地元の小学校の教員になりました。しかし仕事の合間に独学で数学の勉強をし,数学の専門誌に自分のアイディアを投稿し始めたと言われます。ブールのユニークな数学理論は次第に認められるようになり,1849年にはアイルランドのコークにあるクイーンズ大学の数学教授に迎えられ,生涯をその地で過ごしました。(図7)

図7 Boole
もう一つの起爆剤は半導体素子の進歩です。1948年米国ベル電話研究所のショックレー (W. B. Schockley, 1910~1989) によってトランジスタが作られ,それまでの真空管に代わって小型化と小電力化が可能となりました。初期のコンピュータでは独立したトランジスタを一個づつ基板の上にハンダ付けで配置していましたが,間もなくシリコン基板の上に写真製版やプラズマエッチングの技術で多数のトランジスタが構成できるようになり,複雑な電子回路がマイクロチップに収まって,コンピュータは卓上型からポケット型にまで小型化されました。昔のコンピュータは研究所や事務所に一台あって,時間を予約して交代で使っていましたが,いまやパーソナルコンピュータで一人一台が普通という状況になっています.もともと電気で動く機械ですから,人間の命令が分かるはずはないので,間に立って命令の翻訳や伝達をしてくれるソフトウエアが必要です。日本語で思ったように自由にコンピュータを使うことが出来るのは,大勢のソフトウエア技術者が努力を積み重ねてくれた結果です。
パーソナルコンピュータはさらに進んで機械類の自動制御に不可欠のものになりました。分析機器にも大抵付属品として組み込まれています。機械固有のプログラムを自動的に実行してくれるので手がかからず便利ではありますが,自らやり方を反省したり向上したりする訳ではありませんので,時々利用者がこのままで良いのか考えて見る必要があります。しかしソフトウエアを改変するのはかなりの知識が必要で,一般の方は要望を専門技術者に伝えて直して貰うのが賢明です。
3.1.計算目的の多様化
CH重量分析やN容量分析から始まった有機元素分析では,試料量と燃焼ガス中の目的成分量の相対関係を計算すればよいので,筆算でも何とか処理ができました。その後計算能率を上げるため対数計算が導入され,さらに回転式計算機の時代に移行しました。計算が次第に楽になると分析値の計算だけでなく,今出している分析情報がどのくらい確かなのか自問する時代がやってきました。それは第二次大戦のあと米国産業界で起こった品質管理の理論が定量分析の数値評価に入ってきたからです。もともと自動車部品やプラスチック類の品質を一定水準に保つための規正で,一部のデータを抽出し,平均値とばらつきを量的に評価するルールを定めたものです。よく使われたのは「3σ法」で,標準偏差の3倍を超えるものが出ると異常値として生産工程を止め,原因を調査して改善されると再び生産に戻るというものです。これは相当粗いやり方で工業材料にはそれでもよいかと思われますが,定量分析にはもっと細やかな対応が必要でしょう。
標準偏差の計算法はどなたもご存知ですが,n個のデータから平均値X0を求め,各データの平均値からの偏差Xi-X0を計算すると,このデータ群のばらつきが分散Vとして得られます5).標準偏差σは分散の平方根ですから,(5.分析値の信頼性を参照)
V=Σ(Xi-X0)2/(n-1)
∴σ=[Σ(Xi-X0)2/(n-1)]1/2
この理論は計算手段が筆算からやっと手回し計算器に代わった頃に出てきたものですから,有機元素分析では微量はかりの性能評価にまず使われました。当時はナイフエッジ式のはかりが主力で,ザルトリウス,ブンゲ,島津製作所,長計量器などの製品が普及していました。これらを空がけで振らせて読みを10回ほど記録し,標準偏差を求めるのですが,多くのものがσ=2~3μgで,しかも試料の計量には空のボートと試料を載せたボートの差をとるので,試料採取量のばらつきは標準偏差として1.41倍,すなわち2.8~4.2μgということになります。試料量が3 mgほどであれば分析の出発点ですでに1/1000以上の誤差があるわけで,分析誤差に無視できない影響があります。また分析装置全体がうまく働いているかどうかは標準試料を何回か繰り返し分析してその結果を統計処理しますが,これにも標準偏差を求める計算がしばしば行われます。
「分析化学における推計学」という著書も出て5),分析化学者は誰もが統計処理を身につけるようになりましたが,同時に処理の数理も段々複雑になってきました。吸光分析や電気化学分析で検量線が繁用されるようになって,元素分析の領域でも例えばはかりの質量と投影目盛りの読みなどの直線性が吟味されるようになりました.最初は直交座標にデータをプロットして,どの点からもなるべく離れないように直線定規で線を引くという方法が取られましたが,これでは主観が入るというので間もなく最小二乗法による回帰直線を引くという方法に代わりました。これは仮想の直線 y=ax+b を一本引いて,この直線から各プロットが最も近くなるようaとbを決めるというものです。実際には各プロット(yi,xi)と仮想直線との差,すなわちyi-y=yi-axi-bの二乗の合計が最小となるようなaとbを決めることになります。計算過程は少々複雑になりますが,最終的には
a=y0-bx0 (y0,x0は平均値)
b=(Σxiyi-y0Σxi)/(Σxi2-x0Σxi)
で回帰直線が引けます。これを筆算や手回し計算器でやろうとすると半日くらいは掛かってしまいますが,それでも大事な計算ですから我慢してやりました。
幸いなことにこの時代に電子計算機の小型化が進んで,四則演算だけでなく良く使う関数計算の機能を持たせたものが市販されるようになりました。平方根,対数,三角関数などがボタンを押すだけで表示されるので助かりましたが,そのうち統計計算のボタンも設けられ,標準偏差もデータを入れるだけで瞬時に結果が出るようになりました。ポケット電卓では無理ですが,パーソナルコンピュータでは最小二乗法による回帰直線を計算して装置の感度係数まで知らせてくれる便利な時代になりました。
3-2.定量分析の計算 自己積分法のモル分率補正
手回し計算器がまだ一般に使われていた頃,CHN分析をガスクロマト法で実施する方法が学会誌に報告されるようになりました。窒素,二酸化炭素,水の順序でクロマトピークが現れますが,本来各成分量はピーク面積に比例するので,積分計を使って面積を評価しなければなりません。真空管を使った積分計は当時にもありましたが,4桁の精度を出すものは恐ろしく高価なもので,分析装置の付属品にはとても出来ませんでした.1964年最初に市場に出されたF&M 185形の装置6)(図8)では積分計を使わず,ピーク高さ法を採用せざるを得なかったのが実情です.ピーク高さ法では燃焼成分がカラム内で広がっては困るので,試料量を1mg以下に制限し,このため超微量はかりが付属品として組み込まれました。

図8 F&M 185
1962年スイス工科大学のW. Simonによって自己積分法という新しい提案が出て注目されましたが7),ここでは燃焼ガスを真空にしたガラス球にヘリウムと共に収容し,混合希釈したあと,水,二酸化炭素,窒素を含む試料ガスを三対の差動熱伝導度計に拡散させ,それぞれの持続的な差信号を取り出すようにしています。興味ある原理でしたが,真空ポンプで排気したり,ガラス球の圧力を監視したり,あちこちの活栓を操作したりで,とても自動分析装置に仕立てられそうにありませんでした。ただ燃焼ガスを希釈するのでクロマト方式のように試料量を1mg以下に制限する必要がなく,また何よりも持続信号を測定するので積分計が不要という大きなメリットがありました。
それでも自己積分法の長所を生かして機械化ができないかと取り組んだ研究がわが国と米国で非公開の内に進められ,1965年のペンシルバニア州立大学における国際微量化学シンポジウムで同時に発表されました8,9)。このあたりの事情は本微量分析関連記事「9.ポンプシステムが支えるCHN分析計」にやや詳しく書いてありますので参考にして下さい。積分計が不要で,検出器の持続的出力を測ればよいという原理からすると,分析値の計算は甚だ簡単で,標準試料を使って出力1カウント当たりの元素量μg/count(感度係数)を求めておけば,未知試料のカウント数に感度係数を乗じて元素量が計算出来ます。大雑把な分析値であればこのままで良いのですが,差動熱伝導度方式では入口側と出口側セルの間で測定成分の除去があるので,出口側セルの中の成分モル分率が僅か変動しています。計算によって変動しなかった時の値に修正することが出来るのですが,かなり複雑な計算式になりますので,予め計算しておいたモル分率補正係数表を利用することとしました.まだ手回し計算器の時代ですから,なるべく簡単なものが望まれました。
補正計算については本ホームページ「10.熱伝導度セルのはたらき; 3.非検出成分の妨害」に考え方を図で説明しましたが,少し数理的に立証してみたいと思います2)。今検出器の入口側と出口側の間で燃焼ガス中i成分が除去されたとして,もし他成分のモル分率が変わらないと仮定すれば,熱伝導度差Δλは,
Δλ= Xi(λHe―λi)
です.ここでXiは除去されたi成分のモル分率,λHeとλiはそれぞれヘリウムとi成分の熱伝導度です。ゆえにΔλは除去された成分のモル分率Xiに単純に比例します。しかしH検出器では水が除去され,C検出器では二酸化炭素が除去され,N検出器では窒素が失われていますから,熱伝導度差は除去された成分のモル分率に単純には比例しません。今水,二酸化炭素,窒素各検出器で除去された成分のモル分率をXH, XC, XNとし,λHe-λiをλH,λC, λNで表せば,各検出器での熱伝導度差はかなり面倒な計算を経て,
ΔλH = XHλH ―[XH/(1―XH)]×(XCλC+XNλN)
ΔλC = XCλC/(1―XH) ― XCXNλN/[(1―XH)(1―XH―XC)]
ΔλN = XNλN/(1―XH―XC)
の式で表されることが分かりました。他成分の存在によって複雑な形の式になってしまいましたが,単成分の時の熱伝導度差に換算しようとすると,単成分/混合成分の比を補正係数として掛ければよいことになります。
さて補正係数を実際の数値として求めるに当たっては,現実にポンプ内の各成分のモル分率がどの位の値になるのか知っておかなければなりません。微量分析では試料の量が2~3 mgで,この中の元素量はH=10%,C=90%,N=40%あたりが上限ですから,それぞれH=0~200μg,C=0~2000μg,N=0~1000μgを考えておけばよいでしょう。元素量から水,二酸化炭素,窒素の質量Qiμgが計算できますから,その分子量をMiとするとQi/Miでモル数(μmol)が分かります。今ポンプ容量をV ml,温度をT℃,気圧をP mmHgとするとモル分率は,
Xi=(Qi×10-3/Mi)×22.4×(T+273)×760/(VP×273)
ですが,T=55℃,V=150 ml,P=760 mmHgとすれば,
Xi=(Qi/Mi)×10-3 ×0.1794
となります。例えば炭素1000μgからQC=1000×(44.01/12.00)=3667μgの二酸化炭素が生成しますから,QC/MC=83.32μmolとなり,XC=0.01495が得られます。モル分率0.01495とはポンプ内での体積濃度で1.495%ですから,熱伝導度計の直線範囲の良いところにあります。色々の値のXiを求めておいて,Δλ/Δλiの比を表にしたのが補正係数表で,本ホームページの「10.熱伝導度セルのはたらき」に掲載してあります。
この補正表を作るための計算は手回しの計算器を使って行われましたが,随分手間がかかり,検算も含めて一月ほどかかりました。ステップを細かくするともっと精密な表になりますが,使うほうで数値を探すのが面倒になりますから,当時通用していた±0.3%の分析許容誤差に目立った影響が出ないようステップを調節しました。しかし後になってステップの中間の値が欲しいという方もあり,自身で中間値を内挿して頂きました。とにかくこの補正表は手回し計算器の時代から,電卓時代に入ってもかなり長い間利用されました。
3-3.定量分析の計算 モル分率補正法の改革
最初に出来たモル分率補正表は,明らかな誤差要因を解消しようというのが目的で,この点では当面の役割を果たしたと思われます。しかし現在から見ればかなり荒削りなやり方で,その後いろいろ不完全な点が指摘され,改善の努力がなされました。まず1980年代に入るとパーソナルコンピュータが普及してきて,補正表から数値を探すのでなく,近似式を組み立ててデータを入れればすぐ補正係数が得られるようになりました。
FH=1.005+1×10-5×Cμg
FC=1.000176-9.968×10-5×Hμg+6.934×10-6×Nμg
FN=0.99977-1×10-4×Hμg―1.642×10-5×Cμg
この近似式は理論に基づいたものではなく,補正係数表の数値に出来るだけ近い値がでるように試行錯誤で作ったものです。もともと荒削りな作業で出来た補正係数表を基にしていますから,この式も多少信頼性に欠ける面がありますが,連続値が得られるのでステップ間にある不連続性は無くなりました。
この頃関西地区で微量分析ミニサロンが開催されるようになり(第1回は1981年),そのうち自己積分法CHN分析計のモル分率補正に関連した問題について議論が起こりました。それはある標準試料で感度係数を定め,同じ標準試料を未知試料と考えて分析値を求めると元の理論値に正確には一致しないと言うことです。これはモル分率補正の計算が近似値で行われている結果で,当然起こる現象と言えます.例えばアンチピリン2092μgを燃焼し,次のデータを得たとします。
YH=9088 counts YC=10764 counts YN=9636 counts
各成分元素の含有率はH=6.43%, C=70.19%, N=14.88%ですから,
QH=134.5μg QC=1468.4μg QN=311.3μg
これからモル分率補正式でFH=1.0197, FC=0.9889,FN=0.9622が得られ,感度係数 (μg/count) は,
SH=QH/(YH×FH)=134.5/(9088×1.0197)=0.01451
SC=QC/(YC×FC)=1468.4/(10764×0.9889)=0.13795
SN=QN/(YN×FN)=311.3/(9636×0.9622)=0.03358
となります。
この感度係数はすでに近似値で出来た補正式を使って計算していますが,これで逆にアンチピリンを未知試料として分析値を求めてみます.各元素の概略量は,
Hμg=YH×SH=9088×0.01451=131.9
Cμg=YC×SC=10764×0.13795=1484.9
Nμg=YN×SN=9636×0.03358=323.6
ですから,モル分率補正係数は,
FH=1.0198 FC=0.9895 FN=0.9622
となり,上記の補正係数と少し違ってきます.これを使って結果を出すと,
H= 6.43% Δ = 0.00%
C= 70.23% Δ=+0.04%
N= 14.88% Δ= 0.00%
のようになり,水素と窒素については殆ど誤差がありませんが,炭素に関しては気になる誤差を生じこれが課題となっていました。
この時期大阪大学の奥宮正和氏と大阪市立大学の合田純一氏が前後してそれぞれの修正案を発表され,モル分率補正計算の欠陥は除かれることになりました10,11)。これが出来るようになったのは全くコンピュータのすぐれた演算能力によるもので,よい時代に出会えたことも幸いしました。計算式もプログラムしておけば複雑なものでも一瞬に結果が出るので,例えば水素のモル分率補正計算に炭素だけでなく窒素の影響も加えるようになりました。
FH=1+15×10-6×Cμg+6×10-6×Nμg
FC=1-89×10-6×Hμg+6×10-6×Nμg
FN=1-89×10-6×Hμg-15×10-6×Cμg
しかしこの新しい式も概算値ですから上の例のようにまだ僅かな分析誤差が出ます。奥宮氏10)はこの誤差を避けるため一度概算の補正係数でH%, C%, N%を求め,これから各元素の質量を計算し,信頼性の向上した元素質量を使ってもう一度モル分率補正係数を求め直せばほぼ正しい値が得られると提案しています。別に考えられる便法として,水素と窒素の誤差が小数以下2桁まで表に出ないことから,先ずH%を出し,これを使ってN%を計算,これらを使って最後にC%の計算をするとかなり誤差が小さくなるという巧妙な方法も提案しています。いずれの方法も数理的にはまだ誤差がゼロとはなりませんが,日常分析には殆ど支障が無くなります。モル分率補正の数理問題とは少し外れますが,燃焼管,ポンプその他の流路系における水の吸脱着や検出器の非直線性の影響があり,奥宮氏はこれらを配慮した計算式の微修正も提案されていますが,本稿ではスペースの関係もあり別の機会に譲りたいと思います。
一方合田氏 は1973年よりパーキンエルマ240形を運用されていましたが,この装置は燃焼ガスをヘリウムと共に300 mlのガラス球に1500 mmHgまで圧入し,あと差動熱伝導度計で検出する方式ですから原理的にはモル分率補正が必要です。しかしガラス球が大きいことと2気圧ほどに加圧するので燃焼ガスの希釈率が高く,モル分率補正は省略されていました。実用的にはこれで差し支えなかったのですが,コンピュータ時代になって計算が便利になり,僅かな誤差も除けるものは排除しようと,1983年にパーキンエルマ用モル分率補正計算のプログラムを作成されました。コンピュータ計算ですから相当複雑なものでも一瞬に終わるので,モル分率補正計算を3度繰り返し,数理的にも限りなく誤差をゼロに近づけることが出来ました。このプログラムの入ったソフトは同じ装置を使っている国内の他の分析室にも配布され,分析精度の向上に貢献しました。その後11), 1993年と翌年に行われた微量分析ミニサロンでの質疑に応じる形で,上のプログラムに気圧補正を加えたCHNコーダー用プログラムを作成されました。
3-4.定量分析の計算 モル分率補正式の直接解法
モル分率補正の計算は手回し計算器の時代から始まり,当時は面倒でも±0.3%の許容誤差を維持するために仕方なく行っていたと言えます。検出器の出力もチャート紙上のペンの振れ幅をバーニア目盛り付きのノギスで0.1 mm単位まで読んでいましたから,読み方に個人差があり,また転記ミスにも気を使いました。電子装置の進歩でまもなく出力をデジタル化してプリントさせるものが現れ,(図9) これを利用することで個人差や数字の読み間違いなどが無くなりました。さらに演算機能を持ったパーソナルコンピュータが現れて,モル分率補正も数値表を探さず数式をプログラムに組み込んで補正値を求めるようになったのは上述の通りです。時代が進むとコンピュータはデータ処理だけでなく,分析装置の運転にも関わるようになり,キャリヤーガスのOn-Offから加熱装置の温度制御,ポンプの動作,検出器出力のモニタリングなどを自動的に行うと同時にそれらの表示をする要求も出てきました。

図9 デジタルプリンタ
日本エクスラン工業(株)からこれらの要求を充たすコンピュータソフトの支援が得られることになり,これによってパネルディスプレイを含むCHN分析計が構築されました。この内モル分率補正に関しては初期の補正式を踏襲していましたが,まもなく上記の議論が討論会などに出てきましたので,何らかの対応を迫られました。近似式を使って補正を2回または3回繰り返すという言わば「漸近法」も採用を検討されましたが,たまたま同社の安東浩司氏がH,C,Nに関するモル分率補正式を連立方程式として解く方法を見つけ,これによって全く誤差の出ない計算法が考え出されました12)。この解法はかなり複雑な数式の操作がありますのでここでは説明を省略しますが,結論としては各元素の質量として次の3式が得られました。
QH=SHYH’×λH/(λH-ΦCSCYC’λC―ΦNSNYN’λN)
QC=SCYC’×λC(1―ΦHQH)/(λC―ΦNSNYN’λN)
QN=SNYN’×(1―ΦHQH―ΦCQC)
ここでY’=Y×(P/760)でシグナルを1気圧に換算,またΦは装置定数でポンプの温度,圧力,ガスの熱伝導度などを読み込んで,例えばΦH=8.903×10-5, ΦC=1.4945×10-5,ΦN=0.6408×10-5のような値になります。
これらの式を見ると面白いことに気がつきます。Nの式にはYH’やYC’のシグナルがありません。標準試料を使ってYN’と各元素の質量を入れると感度係数SNが決まります。SNが決まるとCの式に代入して,あとYC’ や各元素量を入れれば残りのSCが計算できます。最後にHの式でSNとSCの値を入れるとSHが求められます.次にこのようにして得た各成分の感度係数を使って未知試料の分析を実施しますが,まずHの式にシグナルYH’, YC’, YN’を入れてQHを求め,この値をCの式に入れて同様にQCを計算,さらにQH, QCをNの式に入れてQNが得られます。これらの値にはすべてモル分率補正の計算がされているので,単成分の時に得られる測定値と同じになります。また標準試料を用いた感度係数の算定と,この感度係数を使った同じ標準試料の元素分析値は同じ計算方程式に基づいているので理論値に完全に一致します。実用面で言えば補正計算を繰り返す漸近法も連立方程式の解法によるものも同じ分析結果に到達するので,どちらを選択しても良かったのですが,数理的に直接的な後者のほうで現在は計算ソフトが設計されています。
4-1.おわりに
半世紀の間に起こった計算法の進歩は定量分析の方法にまで影響が及びました。手計算では一日かかりそうな計算がコンピュータでは一瞬で終わるので,早いというだけでなく,気軽に贅沢な計算式を使って結果を出しています。最小二乗法による検量線の作成や繰り返しデータの標準偏差なども手計算では随分時間がかかりますが,電子計算では基礎データがあればボタン一押しで表示され,途中経過での入力ミスも起こりません。
計算に使われるハードウエアは電子機器で,命令さえすれば忠実に実行してくれますが,命令の内容は人間の頭脳が決めるので,これがうまく目的に適合していなくてはなりません。また命令が電子計算機に理解できることも大切で,初期のコンピュータでは計算させるためのプログラム作りが一苦労でした。機械語やフォートランなど近づき難い言語でのソフトも初期には使われましたが,間もなくベーシックによる計算プログラムがパーソナルコンピュータで使えるのようになって,情報科学の専門家以外でもある程度勉強すれば簡単な計算ソフトが組めるようになり,分析化学者の中には結構堪能な方も出てきました。
差動熱伝導度法の装置に特有なモル分率補正はクロマト法の装置にない仕事ですが,これを克服することで検出器は持続的な信号を読み取ればよいことになり,測定上大きなメリットになりました。補正の数理は多少複雑でしたが,初期の段階ではなるべく分析者の負担にならないよう,結果だけを簡略な数値表として提供しました。手計算の時代でしたからこれも止むを得ない選択であったと思います。しかし時代はこの分析装置に合わせたように電子時代に突入し,出力のデジタル表示やプリンタを備えた小型コンピュータが出始め,これらが年を追って能力を高め,遂にパーソナルコンピュータとなって複雑な補正計算も瞬時に実行出来るようになりました。時代はさらに進んで装置全体をコンピュタータが動かすようになりましたが,これらは分析者,装置技術者,ソフト技術者の相互協力があっての賜物です。
コンピュータ技術はハード,ソフト共に驚くべき速度で進歩発展を遂げています.分析化学とはもともと違う領域の科学でしたが,その情報処理能力の高さによって今やコンピュータ無しでは殆ど分析化学の仕事が出来なくなっています。ただ注意すべきは情報を発信しているのは分析化学反応物質であって,ここに間違いがあっては如何に巧妙に便利に情報を処理しても空しい結果を招くしかありません。コンピュータによるデータ処理の見事さに心を奪われて,背後にある分析化学反応の持ついろいろな問題点の探索と解決の努力を忘れてはなりません。
5-1.参考文献
1)F. Pregl:”Die quantitative organische Mikroanalyse”, Springer, Wien (1910).
2)日本分析化学会有機微量分析研究懇談会:“有機微量定量分析”,p754,南江堂 (1969).
3)JIS-Z8101 (ISO 3534):“統計―用語と記号”,日本規格協会(1999).
4)日本規格協会編:“質量の精密測定マニュアル”,p242,日本規格協会(1981).
5)小島次雄:“分析化学における推計学”,基礎分析化学講座5,共立出版(1965).
6)O. N. Hinsvark, R. H. Walts:F&M Scientific Corp., Technical Paper, 31 (1964).
7)J. T. Clerc, R. Dohner, W. Sauter, W.Simon:Helv. Chim. Acta,46 , 2369 ( 1963).
8)K. Hozumi:Microchem. J., 10, 46 (1966).
9)R. D. Condon:Microchem. J., 10, 408 (1966).
10) 奥宮正和:“技法の応用とCHN分析の諸問題”,有機微量分析研究懇談会 (1986).
11)合田純一:阪大,市大分析者の会 (1995).
12)安東浩司,森沢伸一,穂積啓一郎:分析化学,46, 627 (1997).

